晚期卵巢癌患者PARP抑制剂一线维持治疗需全面评估、综合管理
时间:2021/11/30 11:04:49 作者:钟兰
初始治疗 BRCA野生型 高复发风险 满意肿瘤细胞减灭术 新辅助化疗 PARPi单药治疗*仅供医学专业人士阅读参考



 00:000:00
病例介绍
00:000:00
病例介绍


 00:000:00
专家点评
00:000:00
专家点评
维持治疗是卵巢癌治疗全程管理的重要组成部分,PARP抑制剂的问世是卵巢癌治疗领域的重大进步。一系列高级别循证医学证据表明,PARP抑制剂维持治疗显著推迟患者复发时间,延长无进展生存(PFS)时间。那么对于达到满意切除术但仍有残留癌灶<1 cm的患者,化疗达完全/部分缓解(CR/PR)后是否可启用尼拉帕利维持治疗?疗效和安全性如何?如何平衡有效性与安全性?以下的病例将为我们分享尼拉帕利在真实世界中的临床应用经验。
病例回顾
基本资料
患者,女性,确诊卵巢癌的年龄为62岁,既往有高血压病史,否认家族恶性肿瘤史。
治疗经过
✔第一阶段:新辅助化疗+手术+术后化疗
患者2018年5月出现无明显诱因全腹钝痛,当地医院就诊,B超检查示“双侧附件囊实性包块,性质待查”。遂至我院就诊,查体,生命体征平稳,一般状况良好,二便基本正常。专科查体:右附件区扪及约4 cm包块,质中,活动欠佳,无压痛,左附件区增厚,无压痛,移动性音可疑阳性。CT检查提示:右附件3.8×3.3 cm囊实性占位,腹膜增厚,肝肾间隙、脾肾间隙旁、大网膜及左侧结肠旁沟腹膜增厚,局部见小结节影,腹盆腔少量积液,考虑肿瘤种植转移可能(图1)。肿瘤标记物血CA125 2833.503 U/ml。行腹腔穿刺,抽出血性腹水200 ml,送病检,查见腺癌细胞。CT的Suidan评分>3分。
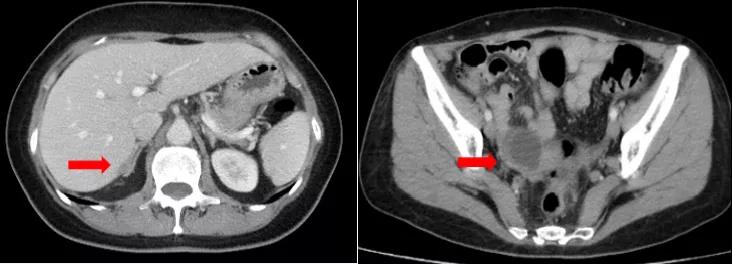
图1. 入院时CT检查结果
初步诊断:盆腹腔恶性肿瘤;恶性腹水;高血压。
经多学科(MDT)讨论,评估手术达R0可能性小,决定先行新辅助化疗2~4周期后评估肿瘤细胞减灭术时机。完善化疗前准备后予紫杉醇+卡铂方案化疗4周期。3周后开腹行“卵巢癌肿瘤细胞减灭术(全子宫切除术+双侧附件切除术+恶性肿瘤细胞减灭术+大网膜切除术+肠粘连松解术+输尿管粘连松解术+乙状结肠肿瘤切除术+乙状结肠修补术+直肠部分切除术+直肠吻合术小肠肿瘤切除术+小肠吻合术+小肠浆肌层修补术+阑尾切除术+回肠预防性造瘘术)”。术后达R1(残留肿瘤部位及大小:乙状结肠壁粟粒样结节,单个病灶直径小于0.5 cm)。
术后病理:(左、右卵巢)高级别浆液性腺癌;癌累及(左、右)输卵管、(左)盆侧壁手术切缘、(大网膜)、(乙状结肠肿瘤)、(小肠肿瘤)、(直肠肿瘤)、(右结肠旁沟腹膜肿瘤)及阑尾。癌未累及子宫、(右)盆侧壁手术切缘、送检(小肠肿瘤)肠管两端切缘及(直肠肿瘤)肠管两端切缘。IHC:CK7(+)、CK20(-)、CA125(+)、P53(+)、WT-1(+)、P16(+)、ER(+)、PR(灶性+)、Ki-67阳性率约30%。
术后最终诊断:卵巢高级别浆液性腺癌新辅助化疗肿瘤细胞减灭术后ⅢC期(R1)。
术后8天行紫杉醇+卡铂方案化疗6周期(患者拒绝使用贝伐珠单抗),末次化疗时间为2019年3月11日,CA125为4 U/ml。化疗中期和结束后,复查CT均未见异常,根据RECIST1.1标准评估达CR。
✔第二阶段:PARP抑制剂维持治疗
患者术后行了基因检测,结果显示:BRCA无致病突变,未测HRD。自2019年5月起口服尼拉帕利200 mg qd至今,期间曾出现Ⅰ~Ⅱ级恶心、呕吐等胃肠道反应,未来院处理,1月后症状逐渐消失;曾出现Ⅱ度白细胞减少、粒细胞减少;γ-GT轻度升高,以上不良反应均未进行特殊处理,尼拉帕利剂量未调整且无用药中断。维持治疗期间CA125波动在正常范围(图2)。2019年10月24日查PET-CT未见确切肿瘤残留及复发征象。
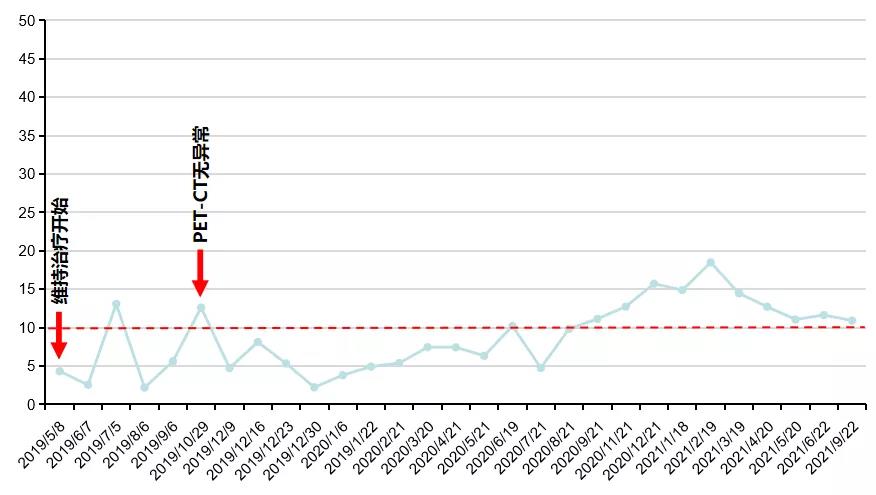
图2. 维持治疗期间CA125变化情况
病例总结
患者无明显诱因出现全腹钝痛,B超提示:双侧附件囊实性包块性质待查。遂来院就诊,综合查体、各项检验、检查结果提示盆腹腔恶性肿瘤,经MDT讨论后先行新辅助化疗4周期后行了肿瘤细胞减灭术,手术达R1,术后诊断:卵巢高级别浆液性腺癌新辅助化疗后ⅢC期(R1)。术后行紫杉醇+卡铂方案化疗6周期,CA125降至正常,RECIST评估达CR。患者的BRCA(-),于2019年5月开始口服尼拉帕利至今,期间曾出现轻度不良反应,均未处理,未调整尼拉帕利剂量,维持治疗期间CA125波动在正常范围,复查PET-CT未见确切肿瘤残留及复发征象。
专家点评
晚期卵巢癌的初始治疗非常重要,R0切除是我们追求的目标。对于经过影像和/或腹腔镜评估无法达到R0切除的患者,可以采用新辅助化疗后再行间歇性肿瘤细胞减灭术。晚期卵巢癌患者的主要预后因素是术后残留病变的大小,最佳肿瘤细胞减灭术(无肉眼残留病变)患者的总生存期(OS)与残留病变患者相比有显著差异[1]。满意的肿瘤细胞减灭术的标准为术后最大残留肿瘤直径<1 cm[2]。新辅助化疗后行中间型肿瘤细胞减灭术作为初始治疗,能降低肿瘤负荷,提高满意肿瘤细胞减灭术的机率,减少术后并发症和器官切除率,但对患者生存期并无显著获益[3]。本例患者在入院后经MDT讨论评估,采用新辅助化疗+中间性肿瘤细胞减灭术+术后辅助化疗,手术结局为R1,达到满意肿瘤细胞减灭术,术后辅助化疗结束后评估患者达CR,且BRCA(-),患者非遗传性卵巢癌。接下来的治疗方案如何选择呢?
众所周知,维持治疗是卵巢癌治疗全程管理的重要组成部分,指对完成初始化疗达到临床CR或PR的患者给予后续治疗。PARP抑制剂的临床应用建立了卵巢癌维持治疗的新模式,显著推迟了患者复发时间,延长PFS。尼拉帕利PRIMA研究纳入的是具有高复发风险的患者,无论BRCA突变状态,HRD状态为随机分层因素。在总体人群中,尼拉帕利组较安慰剂组降低38%的疾病进展或死亡风险(mPFS 13.8个月vs.8.2个月;HR 0.62,95%CI 0.50~0.76)。同时,在不同生物标志物的亚组分析中,均可看到尼拉帕利组有不同程度获益。该研究支持尼拉帕利用于BRCA突变、没有BRCA突变或HRD阴性的患者,即所有上皮性卵巢癌患者的一线维持治疗[4]。本例患者尼拉帕利维持治疗已2年,目前仍为CR。
PARP抑制剂与细胞毒性化疗药物相比不良反应有差异,需严格管理,特别是要注意贫血、血小板减少和其他重要脏器的损害,特别是罕见的骨髓增生异常综合症(MDS)和继发性急性髓系白血病(AML),在维持治疗期间应定期评估疗效与安全性,还应加强患者教育、定期随访,定期监测血常规,观察贫血、血小板减少、疲劳、恶心和呕吐、疲乏等不良反应[4]。临床医生需全面了解PARP抑制剂的特点、配伍禁忌、药物不良反应等问题,加强患者长期治疗管理,提高用药依从性,在必要时提请MDT团队共同处理毒副反应,患者更大程度的获益同时尽可能保障其安全性。
参考文献
[1] Antonio González-Martín,et al. First-Line and Maintenance Therapy for Ovarian Cancer: Current Status and Future Directions. Drugs. 2014 Jun;74(8):879-89.
[2] 中国抗癌协会妇科肿瘤专业委员会. 卵巢恶性肿瘤诊断与治疗指南(第四版). 中国实用妇科与产科杂志. 2018, 34(7): 739-749.
[3] 杨利娟,等.新辅助化疗与初始肿瘤细胞减灭术治疗晚期卵巢癌疗效的系统评价. 中国实用妇科与产科杂志, 2017,33(2): 171-176.
[4] 中华医学会妇科肿瘤学分会. 卵巢癌PARP抑制剂临床应用指南.现代妇产科进展. 2020, 29(5): 321-328.
阅读量:3188 | 点赞量:0
-

分享
-

收藏

 3188
3188