【导读】
•PRIMA研究数据公布,HRp亚组PFS及OS均无长期获益,提示卵巢癌一线维持治疗应精准。
•奥拉帕利仍是目前唯一*在一线卵巢癌的维持治疗领域唯一一个具有两个临床意义OS获益的PAPR抑制剂。
•在合成致死机制中,过强的捕获能力可能增加骨髓毒性,影响临床效果。奥拉帕利在抑制PARP酶活性方面表现优异,临床效果显著。
卵巢癌早诊难、分期晚、易复发,PARP抑制剂的出现打破了卵巢癌反复复发的治疗困局,使卵巢癌患者的生存时间不断延长[1,2]。
此次ESMO大会带来了PARP抑制剂的最新研究结果。我们有幸邀请到同济大学附属东方医院的程静新教授,深入解读此次大会上的研究成果。
一
本次ESMO大会发布关于PARP抑制剂的相关研究为我们提供了何种新见解?
程静新教授:2024年9月ESMO大会中最令人期待的是PRIMA研究最终结果。既往结果表明,尼拉帕利在同源重组缺陷(HRD)阳性(HRD+)或HRD阴性(HRD-)的患者都展示了有临床和统计学意义的中位无进展生存期(mPFS)延长,这也是FDA和我国批准尼拉帕利用于卵巢癌含铂化疗后达到完全缓解/部分缓解(CR/PR)后一线维持治疗的重要依据[3]。此次ESMO大会PRIMA研究最终分析进一步证实了尼拉帕利对HRD+和同源重组功能正常(HRp)患者的mPFS获益。研究显示,尼拉帕利延长随访时间后,HRp亚组5年PFS率8%(vs 安慰剂 7%)。本次披露的OS数据方面,对全人群,尼拉帕利一线维持治疗组与安慰剂之间的OS结果无显著差异,尼拉帕利组中位总生存期(OS):46.6月 vs安慰剂组48.8个月(HR=1.01,95% CI, 0.84-1.23,p=0.8834,数据成熟度:62.5%),且无论患者HRD状态如何,尼拉帕利一线维持治疗组与安慰剂对照组之间OS结果无差异。此外对于BRCAwt的患者而言,接受尼拉帕利一线维持治疗后未获显著生存收益(HR=1.01,95% CI, 0.80-1.27),这一结果表明此类患者接受尼拉帕利一线维持治疗可能对OS存在潜在危害[4]。
PARP抑制剂中,奥拉帕利是临床上使用广泛的药品,其在一线维持治疗中的关键Ⅲ期临床研究有SOLO-1和PAOLA-1。SOLO-1试验纳入BRCA 1/ 2基因致病或疑似致病突变的晚期卵巢癌患者,历经7年随访,奥拉帕利用于BRCAm患者维持治疗的中位OS仍未达到(图1)[5]。而PAOLA-1的OS结果也已经公布,亚组分析显示,无论是否携带BRCA突变,HRD阳性卵巢癌患者接受奥拉帕利联合贝伐珠单抗(BRCAwt亚组及BRCAm亚组)均有临床意义上的OS获益(图2)[6]。奥拉帕利因此是目前唯一*在一线卵巢癌的维持治疗领域唯一一个具有两个临床意义OS获益的PAPR抑制剂。其他PARP抑制剂,如卢卡帕利等一线维持治疗OS数据暂不成熟[7-11]。
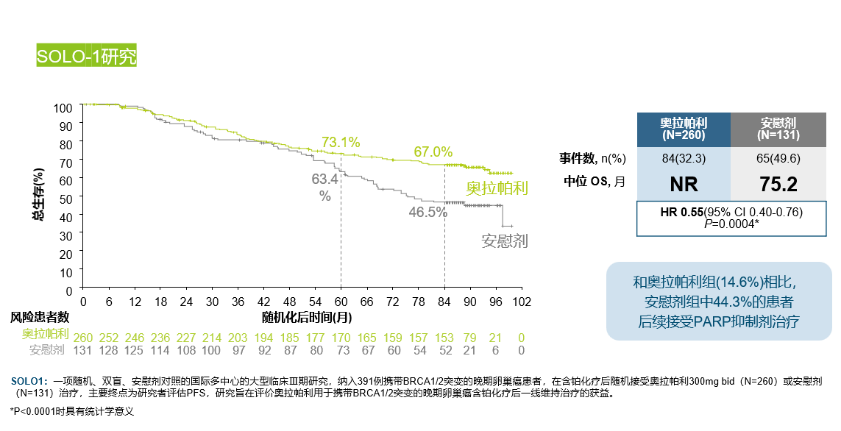
图1. SOLO-1 : 相比于安慰剂,奥拉帕利一线维持治疗晚期卵巢癌可显著降低患者死亡风险[5]
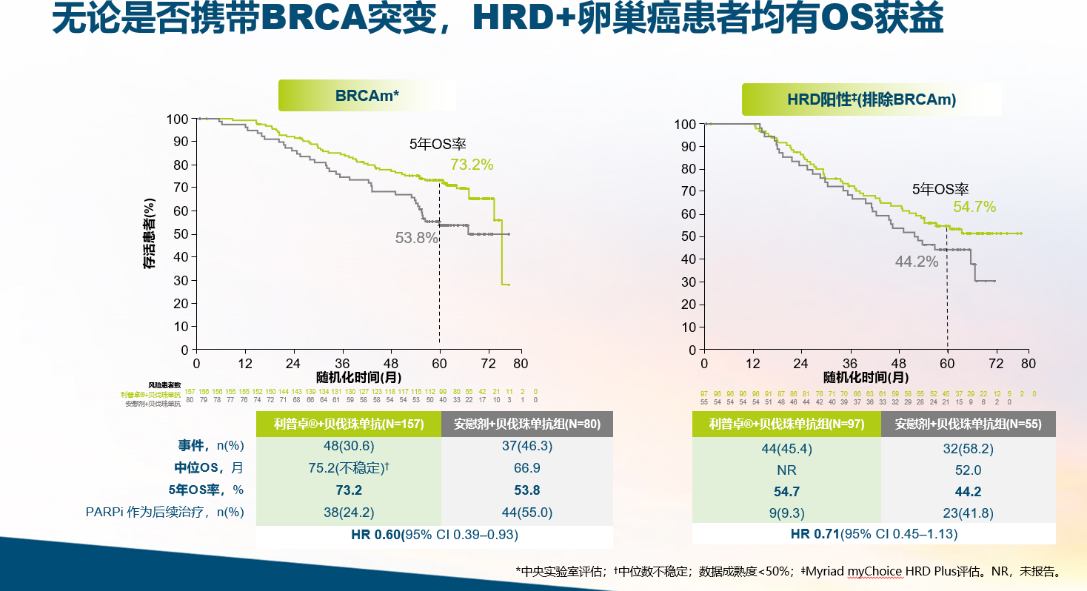
图2. PAOLA-1研究: 无论是否携带BRCA突变,HRD+卵巢癌患者接受奥拉帕利一线维持治疗均有OS获益[6]
PARP抑制剂的OS相关研究提示我们,精准诊疗才能使得卵巢癌一线维持治疗得到更多获益。
二
您能简要解读一下不同PARP抑制剂之间存在不同的药理学基础吗?
程静新教授:目前学界共识PARP抑制剂的主要作用机制是“合成致死“机制[15]。这一机制特别针对DNA修复机制缺陷的癌细胞,PARP抑制剂通过抑制PARP蛋白的催化活性(下简称“催化”)和对PARP的捕获(下简称“捕获”)[12]。
传统观点认为“捕获“是关键,但最新里程碑研究显示,PARP抑制剂的活性与抑制PARP1的活性诱发转录-复制冲突依赖,进而DNA损伤反应水平密切相关[13]。此外,该研究团队发现,仅抑制PARP1酶活性就足以诱导同源重组缺陷细胞的死亡。这说明,PARP抑制剂诱导的“捕获“并不是必要的[16]。
PARP抑制剂中,奥拉帕利对PARP的半抑制浓度仅为1.2nmol/L,远低于维拉帕利和尼拉帕利,对PARP的催化活性有较强的抑制作用[14]。
研究表明,PARP抑制剂的“捕获”能力与骨髓毒性相关,奥拉帕利的捕获能力在PARP抑制剂处于中等水平[14,15]。
在合成致死机制中,PARP抑制剂的“抑制”和“捕获”都重要,但过强的捕获能力可能增加骨髓毒性,影响临床效果。奥拉帕利在抑制PARP酶活性方面表现优异,临床效果显著。未来研究需深入理解合成致死机制,优化药物开发,提高治疗效果。
总结
随着学界对“合成致死“机制的深入研究和临床对 PARP抑制剂的广泛使用,以奥拉帕利为代表的PARP抑制剂使卵巢癌维持治疗进入OS时代。就目前的药理学研究而言,奥拉帕利对于PARP酶催化抑制作用较强,捕获能力在PARP抑制剂中属于中等,是唯一*在卵巢癌中一线维持治疗和PSR维持治疗具有OS获益的PARP抑制剂,且安全性良好。
*唯一:截止至2024年7月,综合ASCO/ESMO大会公布数据以及用关键词advanced ovarian和PARP抑制剂在PubMed数据库搜索临床研究结果。
研究介绍
SOLO1:一项随机、双盲、安慰剂对照的国际多中心的大型临床Ⅲ期研究,纳入391例携带BRCA1/2突变的晚期卵巢癌患者,在含铂化疗后随机接受奥拉帕利300mg bid(N=260)或安慰剂(N=131)治疗,主要终点为研究者评估PFS,研究旨在评价奥拉帕利用于携带BRCA1/2突变的晚期卵巢癌含铂化疗后一线维持治疗的获益。
PAOLA-1研究:一项多国多中心、随机、双盲、3期临床研究,纳入806例一线化疗联合贝伐治疗有反应的新诊断晚期卵巢癌患者,随机分配至接受奥拉帕利300mg bid+贝伐15mg/kg q3w(N=537)或安慰剂+贝伐(N=269)治疗,奥拉帕利或安慰剂的给药持续最长24个月,贝伐给药持续15个月,主要终点为研究者评估的PFS,并由盲法独立中央审查(BICR)进行敏感性分析。
PRIMA研究:PRIMA是一项双盲、随机三期临床研究用于评估尼拉帕利对比安慰剂用于三期或四期卵巢癌患者的一线治疗。该研究通过PFS(无进展生存期)评估尼拉帕利作为维持治疗的有效性。对铂类有应答的患者以2:1比例随机分配至尼拉帕利或安慰剂组。该研究包括了尼拉帕利的个体化使用方案,基线体重<77公斤或血小板计数<150 K/μL的患者接受起始剂量200mg/天进行治疗,其他患者接受300mg/天进行治疗。
安全性真实世界研究:目前最大样本量的不同PARPi真实世界应用对比,纳入在2017年1月1日至2019年5月31日期间813例首次使用PARP抑制剂的卵巢癌患者,其中奥拉帕利303例、尼拉帕利348例和卢卡帕利162例,记录并分析了使用不同PARP抑制剂患者的基线特征、安全性、剂量调整、持续性、依从性、医疗资源利用率和成本等信息。

程静新教授
同济大学东方医院南院妇科主任,妇产科教研室主任,博士生导师
中华医学会肿瘤学分会妇科肿瘤专委会委员
中国老年学会妇科分会副主任委员
中国优生优育学会肿瘤生殖分会常委
中国抗癌学会卵巢癌专委会委员
CSCO妇科分会委员
上海市抗癌学会理事
上海市妇科肿瘤质控专家组成员
上海医学会妇产科分会委员
上海医学会妇科肿瘤分会委员
上海市医师学会妇产科分会委员
上海市抗癌学会妇瘤专委会副主任委员
浦东新区医学会妇科分会副主任委员
《实用妇产科》杂志常务编委
《实用癌症杂志》编委
《中国内镜杂志》编委
从事临床工作近40年,擅长妇科肿瘤及宫颈癌前病变的手术及综合诊疗
扫码进入专栏观看更多精彩内容

阅读量:652
