【关键信息】
(1)“OS”是临床研究中衡量肿瘤治疗疗效的“金标准”。
(2)奥拉帕利是目前唯一一个在卵巢癌一线维持治疗中,兼具PFS和OS临床获益的PARP抑制剂。SOLO1和PAOLA-1研究中,安慰剂组后续使用PARP抑制剂的比例高达44.3%和45.7%,均高于PRIMA研究中的37.8%。
(3)在这种情况下,奥拉帕利仍然在BRCAm和HRD阳性人群中取得一致性的显著的OS获益。
【导读】晚期卵巢癌一线维持治疗的新药物层出不穷,然而真正实现短期和长期均显著获益的药物仍屈指可数。2024年9月,ESMO公布了新诊断的晚期高级别卵巢癌的一线维持治疗领域的新数据,更新整合本领域的系列研究核心数据有助于医生和患者更加全面、准确的理解和选择治疗策略。
一
PARPi较安慰剂治疗的患者PFS和OS均显著延长才是真获益
SOLO1研究结果显示奥拉帕利VS安慰剂组中位PFS分别为56.0个月VS 13.8个月(HR=0.33; 95% CI 0.25~0.43),5年PFS率为48% vs 21%。亚组分析显示,无论术后是否可见卵巢癌残余病灶,无论含铂化疗达到完全或部分缓解,奥拉帕利均可显著延长PFS,OS亦显著获益,中位生存期较安慰剂组显著延长超9个月。在SOLO1研究长达7年的随访过程中,不论外部综合治疗如何变化,奥拉帕利组相对于安慰剂组患者的长期OS获益仍旧明显(7年OS率67% VS 46.5%)。
PAOLA-1研究结果显示奥拉帕利+贝伐组VS安慰剂+贝伐组中位PFS分别为46.8个月 VS 17.6个月(HR=0.41; 95% CI 0.32~0.54)。
PRIMA研究结果显示尼拉帕利VS安慰剂组中位PFS分别为13.8个月VS 8.2个月(HR=0.62; 95% CI 0.50~0.76),5年PFS率为22% VS 12%。在总生存期方面,不论是中位OS还是5年OS率均与安慰剂相当(表1),无论患者HRD状态如何,尼拉帕利维持治疗组与安慰剂对照组之间OS结果无差异,未见患者获益。
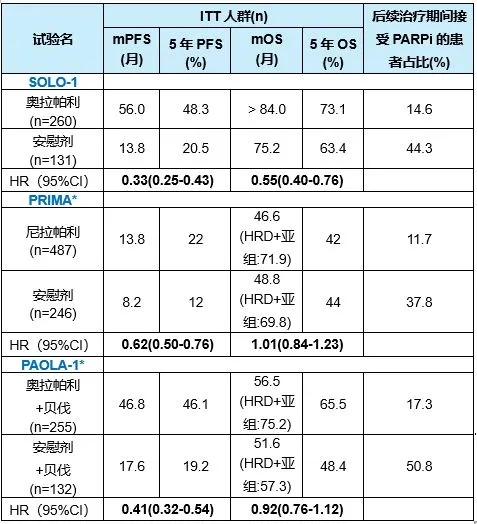
表1. 晚期卵巢癌一线维持治疗研究结果汇总
*PAOLA-1研究的HRD阳性患者中位OS组间差异显著(HR=0.62, 95%CI 0.45-0.85)。PRIMA研究的HRD阳性患者中位OS组间差异不显著(HR=0.96, 95%CI 0.70-1.29)。
二
PARP抑制剂研究亚组人群的获益情况及其与总体获益的一致性
HRD/BRCAm高危卵巢癌患者的一线维持治疗是诊疗的难点,也是药物疗效评估的关键亚组。研究数据显示,SOLO-1研究、PAOLA-1研究和PRIMA研究中BRCAm患者OS的组间比较显示,奥拉帕利相较安慰剂组的HR=0.55(95% CI 0.40-0.76),奥拉帕利+贝伐相较安慰剂+贝伐组的HR=0.62(95% CI 0.45-0.85),尼拉帕利相较安慰剂组的HR=0.94(95% CI 0.63-0.1.41)(图1)。由此可见,奥拉帕利对HRD/BRCAm高危患者仍显著有效与总人群获益趋势一致,而尼拉帕利不仅在总人群中OS与安慰剂无差别,在HRD/BRCAm高危患者人群也没有相对获益。值得注意的是目前中国人群HRD检测普及程度上不高,HRd unknown组反而有明显受损可能(HR 1.39, 95%CI 0.88-2.19)。
此外,尼拉帕利组起始剂量不仅包含固定剂量(FSD, 315/484,65%),还设置了个体化起始剂量(ISD, 169/484,35%),个体化起始剂量通常不足300mg,体现了治疗安全性的平衡可能更为困难。疗效分析显示尼拉帕尼FSD组合ISD组OS与安慰剂的差异仍均不显著(HR 0.95,95% CI 0.75-1.21 VS HR 1.15, 95% CI 0.83-1.60)。
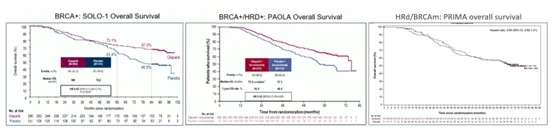
图1. SOLO-1研究、PAOLA-1研究和PRIMA研究中BRCAm患者的OS生存曲线
三
晚期卵巢癌患者PARPi一线维持治疗进展后续治疗的优先选择
PRIMA研究患者疾病进展后的继续接受PARP抑制剂治疗的患者中,入组到尼拉帕利组59.6%(34/57)的患者(其中HRd亚组61.5%(24/36))和安慰剂组57%(53/93)(其中HRd亚组 62.3%(38/61)的患者接受了奥拉帕利治疗,这对整个研究患者OS的延长提供了明显助力。安慰剂组患者进展后,仅31%入组安慰剂治疗的患者选择了跨组使用该项试验药物尼拉帕利(表2)。可以窥见,在欧美人群的临床实践中,临床医生及进展期卵巢癌患者对真正能够改善预后的PARP抑制剂治疗药物之首选为奥拉帕利。
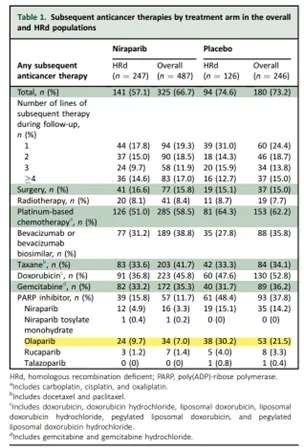
表2. PRIMA研究后续治疗情况
应注意,在SOLO-1和PAOLA-1研究中,安慰剂组同样出现了后续使用PARP抑制剂的情况,且整体交叉比例(SOLO-1的44.3%及PAOLA-1的45.7%)均高于PRIMA研究中的37.8%(图2)。
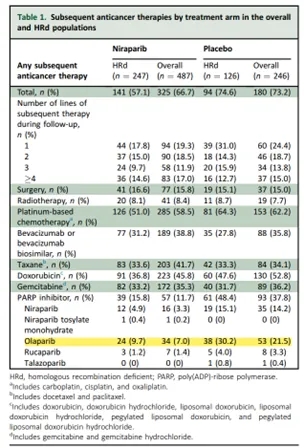
图2. SOLO-1、PAOLA-1和PRIMA中后续使用PARPi情况
随着时间推移,卵巢癌其他综合治疗例如手术质量、新技术等治疗效果不断提高。研究数据显示,其他进展后可能延长OS的序贯治疗,如手术、放射治疗在PRIMA研究中尼拉帕利组和安慰剂组的占比分别为15.8% VS 15.0%,8.4% VS 7.7%,这些因素在两个组分布较均衡,然而尼拉帕利较安慰剂仍无中位OS优势(46.6个月VS 48.8个月)。相比之下,SOLO-1研究的患者多种序贯治疗在奥拉帕利组较安慰组大幅降低,如继续接受PARPi治疗的患者占比分别为14.6% VS 44.3%(表1)。奥拉帕利对晚期卵巢癌患者总生存的优势明显,无惧其他治疗的跨组干扰。

康玫教授
上海市第一人民医院科研处/临床研究中心统计师
中国临床肿瘤学会青年委员会统计小组成员
上海申康医院发展中心临床研究方法学联盟成员
主持上海申康中心研究型医师创新转化能力培训项目(统计师专项)1项,参与国家科技部重点研发计划“病原学与防疫技术体系研究”专项1项、科技部“重大新药创制”专项1项,作为统计师负责人支撑局级重大多中心临床研究项目6项、注册类医疗器械临床试验2项,参与省部级、局级多中心临床研究项目20余项。
发表SCI文章26篇,第一作者论文包括Lancet infectious diseases, Lancet Microbe, Trends in Microbiology, J Clin Endocrinol Metab等, 于Lancet杂志发表临床研究方法学correspondence 1篇,累计IF 180余分。多项研究成果被Lancet infectious diseases引用。
扫码进入专栏观看更多精彩内容

阅读量:1567
